

 Conforme
vimos na aula Racionalismo
e Empirismo, no final do séc. XVIII, o
'século das luzes', vivia-se, na Europa,
o Iluminismo, movimento
cultural-filosófico herdeiro da
tradição do Renascimento
e das concepções mecanicistas da Revolução
Científica e do Humanismo,
defendendo
a valorização do Homem e da
Razão. Acreditava-se
que, aplicado a todas as esferas de
conhecimento e atividade humana, o pensamento
científico levaria ao progresso, ideia que foi
seguida pelo Positivismo
e pela tecnocracia
modernas, como veremos adiante.
Conforme
vimos na aula Racionalismo
e Empirismo, no final do séc. XVIII, o
'século das luzes', vivia-se, na Europa,
o Iluminismo, movimento
cultural-filosófico herdeiro da
tradição do Renascimento
e das concepções mecanicistas da Revolução
Científica e do Humanismo,
defendendo
a valorização do Homem e da
Razão. Acreditava-se
que, aplicado a todas as esferas de
conhecimento e atividade humana, o pensamento
científico levaria ao progresso, ideia que foi
seguida pelo Positivismo
e pela tecnocracia
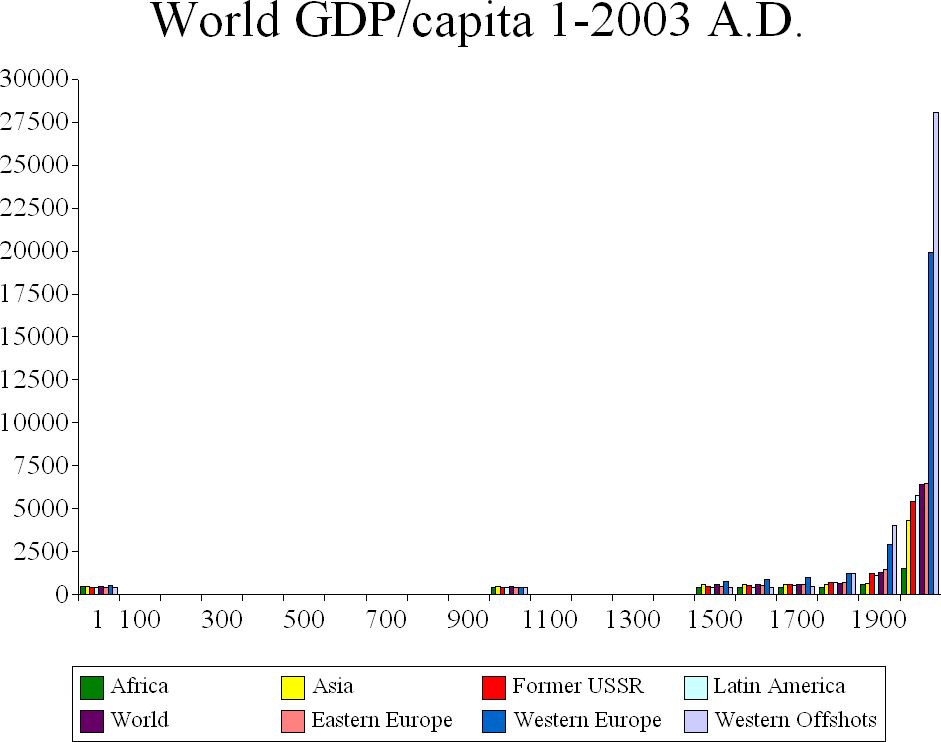
modernas, como veremos adiante.Se o século XVIII foi o século da Mecânica, do estudo das forças, o século XIX foi o da Termodinâmica, o estudo da Energia.
Visto de outra forma,

Antes da Revolução Industrial, vigorava artesanato manual, forma de produção que não deve ser confundida com a atual produção de objetos de cultura popular, em que

Como consequência, a Inglaterra adianta-se 50 anos em relação ao continente europeu em termos de industrialização.
Além disso, sai na frente na expansão colonial para conquistar mercados de matéria-prima e produtos
Finalmente, novas classes sociais aparecem:

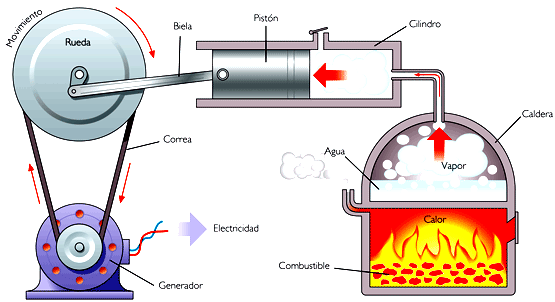
As máquinas a vapor são máquinas térmicas cíclicas que funcionam a partir de uma fonte quente (caldeira) e uma fria (condensador).
Elas derivam do dispositivo denominado eolípila criado por Heron de Alexandria.

 Newcomen foi um vendedor de
ferragens e pregador Batista inglês.
Newcomen foi um vendedor de
ferragens e pregador Batista inglês.Em 1698, construiu a primeira máquina a capturar o poder do vapor para produzir trabalho mecânico.
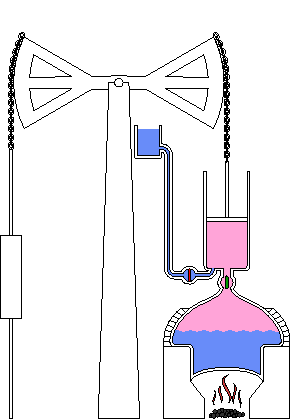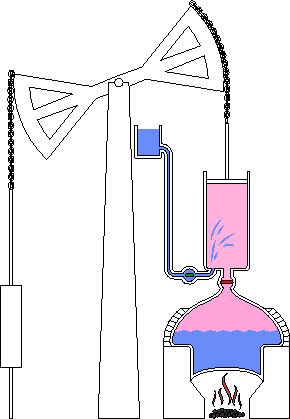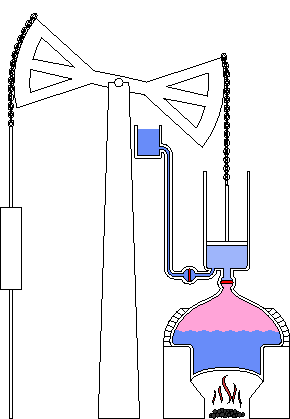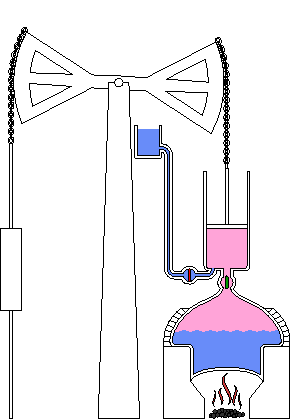
Foi usada principalmente para retirar água de minas de carvão, servindo de base para a mecanização de toda a indústria.

mais uma vez a Física se desenvolve por motivos práticos.
Em 1818, George Stephenson, engenheiro civil e engenheiro mecânico inglês, revolucionou os transportes ao projetar navios e locomotivas a vapor.
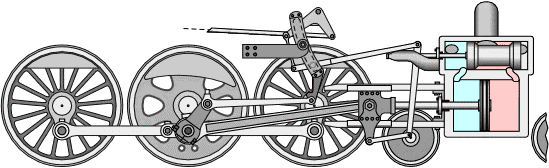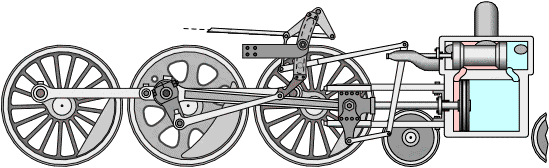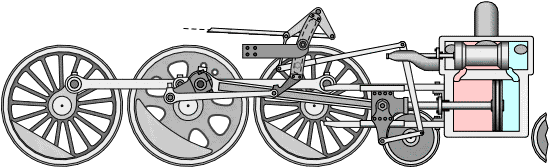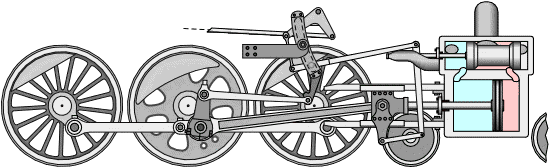
 Rumford, como é mais
conhecido
na Física, foi um físico e
inventor anglo-americano.
Rumford, como é mais
conhecido
na Física, foi um físico e
inventor anglo-americano.Durante a Guerra Civil Americana, foi ativista contra o movimento de independência. Perseguido pelos revoltosos, abandonou esposa e casa e aderiu às tropas britânicas.
Durante este período, estudou o poder da pólvora, o que lhe valeu uma publicação em 1781 no Philosophical Transactions of the Royal Society e a reputação de cientista.
Com o fim da guerra, mudou-se para a Inglaterra, onde recebeu o título de cavaleiro (Sir), posteriormente recebe o título de Conde de Rumford, e casa-se, em 1804, com Marie-Anne Pierette Paulze Lavoisier, viúva de Lavoisier, como vimos na na aula Lavoisier e a Revolução Química.
Enquanto deslocado na Bavária, Rumford observou o calor gerado pela perfuração de canhões no Arsenal de Munique, como se estivessem sendo aquecidos por fogo. Numa experiência, ele colocou o equipamento dentro d'água e observou que, não só a água chegava a ferver, como o suprimento de calor parecia inesgotável, o que era incompatível com a Teoria do calórico, discutida na aula Lavoisier e a Revolução Química. Rumford desenvolve, então, a ideia de que calor é uma forma de energia cinética.

Publicou seus resultados em 1798, em um artigo intitulado An Experimental Enquiry Concerning the Source of the Heat which is Excited by Friction (Uma Investigação Experimental sobre a Fonte de Calor que é Excitada por Fricção), novamente no Philosophical Transactions of the Royal Society. Nele, Rumford argumenta que a única coisa que foi fornecida ao canhão foi o movimento, o que tornou este trabalho fundamental para o estabelecimento do Princípio de Conservação de Energia, embora tenha sido recebido com hostilidade, a princípio.
Embora um pouco tendencioso, este experimento inspirou Joule (vide abaixo) a estabelecer a relação entre energia mecânica e calor.
 Carnot foi um físico,
matemático e
engenheiro francês.
Carnot foi um físico,
matemático e
engenheiro francês.Em 1824, publicou sua obra única Réflexions sur la Puissance Motrice du Feu et sur les Machines Propres a Développer Cette Puissance (Reflexões sobre Potência Motriz do Fogo e Máquinas Próprias para Aumentar essa Potência), onde faz uma revisão das importâncias industrial, política e econômica da máquina a vapor, já bastante utilizada, mas ainda sem um estudo teórico.
Nele, baseado apenas na Teoria do calórico, proposta por Lavoisier em 1783, como vimos na aula Lavoisier e a Revolução Química, Sadi Carnot propos o ciclo conhecido como Ciclo de Carnot, não realizável na prática, mas que se constitui no limite teórico para as máquinas térmicas.
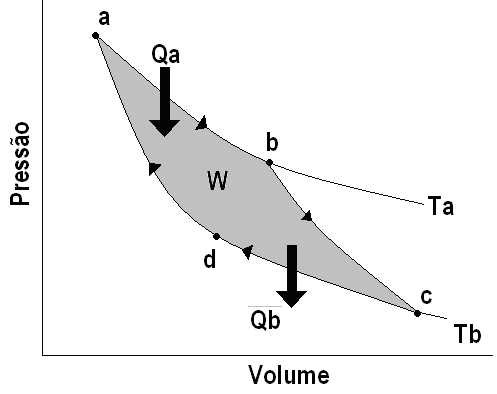
Esse ciclo reflete o Segundo Princípio da Termodinâmica, elaborado por Sadi-Carnot como
"Para haver conversão contínua de calor em trabalho, um sistema deve realizar ciclos entre fontes quentes e frias, continuamente. Em cada ciclo, é retirada uma certa quantidade de calor da fonte quente (energia útil) [Qa], que é parcialmente convertida em trabalho [W], sendo o restante rejeitado para a fonte fria (energia dissipada) [Qb]"
Esse princípio serviu de base para a 2ª Lei da Termodinâmica.
Ela pode ser expressa de várias formas. Uma delas, de forma qualitativa, seria
Não é possível transformar completamente trabalho em calor, sem que outras mudanças ocorram no ambiente.
Na prática,

Como há sempre uma energia dissipada para o meio ambiente em forma de calor, segundo esse princípio, isso implica que não é possível construir uma máquina com rendimento de 100%!
Isso significa, também, que não é possível construir uma máquina que não cause poluição térmica.
Joule colaborou com William Thomson, mais conhecido como Lorde Kelvin no desenvolvimento da escala absoluta de temperatura, hoje denominada escala Kelvin.
Também formulou a lei entre o fluxo de corrente através de uma resistência elétrica e o calor dissipado por ela. Com esse trabalho, ele esperava ingressar na Royal Society, mas como não era engenheiro nem trabalhava na academia, era visto como apenas um amador de província. Felizmente, a história lhe fez justiça e essa lei é hoje chamada de Lei de Joule.
No entanto, sua contribuição mais revolucionária para a Física foi para a Primeira lei da Termodinâmica e para o Princípio de Conservação de Energia, especialmente por seu famoso experimento que demonstra a equivalência entre calor e trabalho.
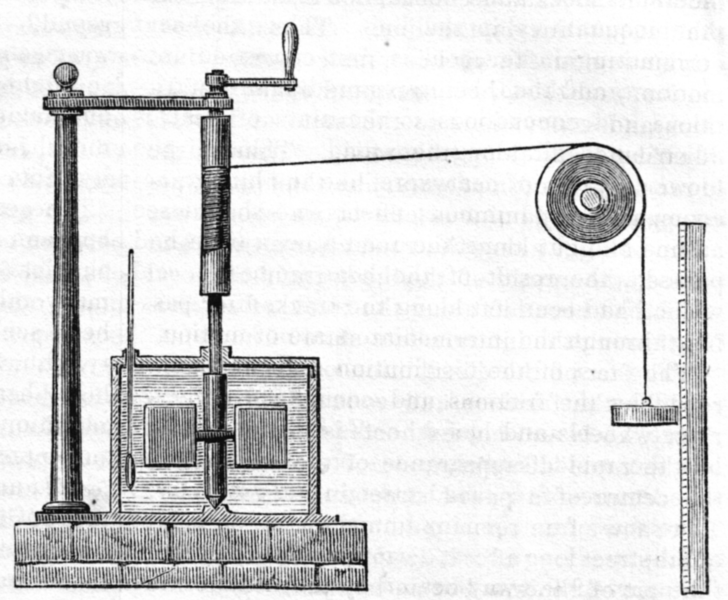
A queda do peso fazia as pás dentro da água girarem, causando um aumento de sua temperatura, pela transformação do trabalho, realizado pela força gravitacional sobre o peso, no calor que, transferido para a água, a aquecia. Joule foi capaz de medir com grande precisão essas duas quantidades e determinou sua equivalência como
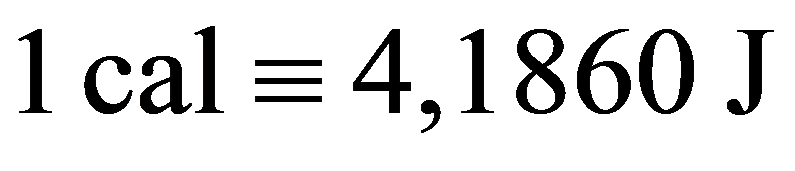
No entanto, a visão de Joule encontrou muita resistência, especialmente por, de forma semelhante ao experimento de rumford, visto acima, implicar num suprimento inesgotável de calórico, aparentemente contradizendo a Teoria do calórico, que até serviu de base para o Ciclo de Carnot, como vimos acima.
 Seus
resultados foram considerados compatíveis com
a Teoria cinética dos gases,
proposta por Daniel Bernoulli, como vimos na
aula A
Revolução na Matemática,
a qual era considerada apenas uma teoria alternativa
à Teoria do calórico.
Seus
resultados foram considerados compatíveis com
a Teoria cinética dos gases,
proposta por Daniel Bernoulli, como vimos na
aula A
Revolução na Matemática,
a qual era considerada apenas uma teoria alternativa
à Teoria do calórico.Em 1850, Clausius demonstrou que era possível compatibilizar o Princípio de Carnot com a Teoria cinética dos gases se a conservação do calórico se transformasse no Princípio de conservação de energia.
Em 1865, Clausius introduziu o conceito de entropia.
Veja também esta página
 Helmholtz foi um médico
e físico
alemão.
Helmholtz foi um médico
e físico
alemão.Helmholtz contribuiu para a Fisiologia e para a Psicologia fisiológica com teorias da percepção visual, visão a cores, percepção do som, etc.
Em 1854, propos a idéia da 'morte térmica' do Universo.
Na Filosofia, é conhecido por sua Filosofia da Ciência, idéias sobre a relação entre as leis da percepção e as leis da natureza, sobre a Estética e idéias sobre o poder civilizador da Ciência também é conhecido como o criador da Teoria da Panspermia Cósmica.
Em 1850, influenciado pela obra Zur Farbenlehre (Da Teoria das Cores), de Goethe (ver abaixo), desenvolveu a teoria de Young, segundo a qual há três tipos de cone na retina: sensíveis ao azul, ao verde e ao vermelho. A intensidade relativa dos sinais de cada conjunto de cones, é interpretada pela mente como cor:
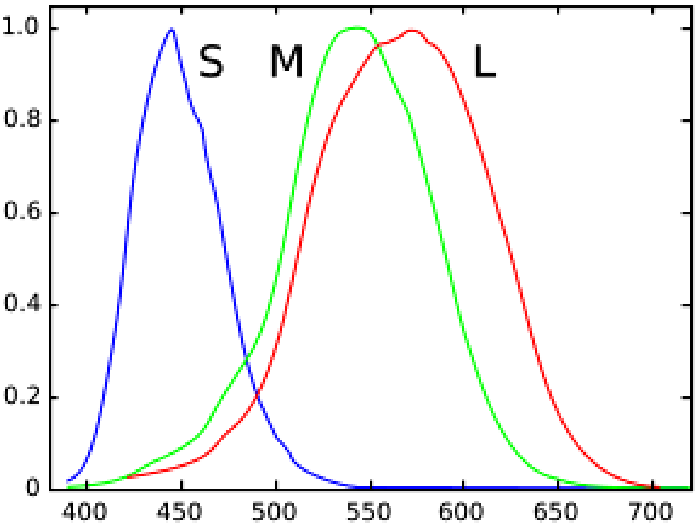
Veja também esta página
Na Física, Helmholtz é conhecido pelas suas teorias da conservação da energia, trabalhos em Eletrodinâmica, Termodinâmica Química e numa fundação mecânica para a Termodinâmica.
Helmholtz chegou ao Princípio de conservação de energia estudando metabolismo muscular. Ele tentou demonstrar que nenhuma energia é perdida no movimento muscular, motivado pela implicação de que não havia 'forças vitais' envolvidas, conceito da tradição especulativa da Naturphilosophie, paradigma dominante na Fisiologia germânica da época, e que se opunha ao mecanicismo newtoniano.
Em 1847, publica a definição definitiva da conservação da energia, na forma da 1ª Lei da Termodinâmica:
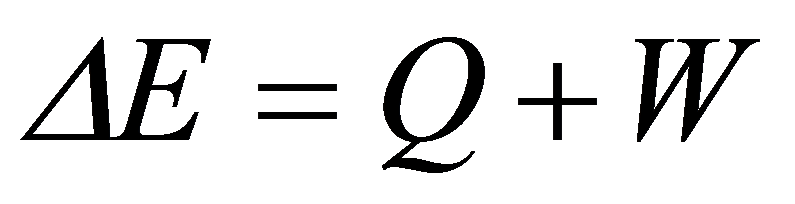
onde
Voltar à Parte Anterior
Voltar a Minhas Aulas.
Voltar ao começo desta página
Voltar à página principal de Física Interessante